全球医疗器械检测认证要求大汇总

全球医疗器械检测认证要求大汇总
欧盟指令中涵括许多基本保健及安全规定,以及评估产品符合规定程度的订定程序。每项指令在区域性标准制订机构所订定的调和欧洲标准中均会具体说明详细的基本规定。
医疗器械标准

这些医疗器械标准已被许多国家广泛采用。
医疗器械指令列表


形成“新方法”基础的指令,包含了广泛的产品类别(横向指令)或某种特定的产品类别(纵向指令)。
欧盟
所有进入欧盟市场的产品,企业必须具有表示自我符合声明的CE标志,以说明产品符合欧盟制定的相关指令。
医疗器械需要满足的指令有:
《有源植入性医疗器械指令》(AIMDD, 90/385/EEC)、《医疗器械指令》(MDD,93/42/EEC)、体外诊断器械指令(IVDD, 98/79/EC)。
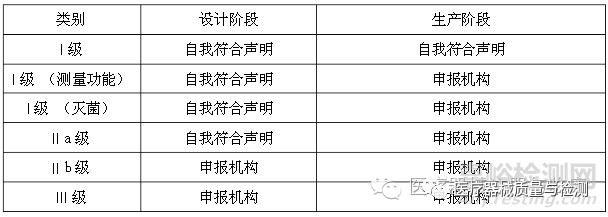
医疗器械指令(MDD),MDD指令适用于大多数进入欧盟销售的医疗设备。它根据不同的要求共分为6个等级,供认证机构评估。
2017 年4 月5 日,欧洲议会和理事会正式签发了欧盟关于医疗器械第2017/745 号法规(MDR,EU2017/745),5月5日,欧盟官方期刊(Official Journal of the EuropeanUnion) 正式发布该法规。2017 年5 月25 日,MDR 正式生效, 替代了原医疗器械指令(MDD,93/42/EEC)和主动植入式医疗器械指令(AIMD,90/385/EEC)。详情请参考《欧盟医疗器械新法规MDR主要变化情况介绍》
认证机构的统一评估包括根据指令规定的基本要求评审技术文件、根据标准EN 46001或EN/ISO 13485评审质量体系。
由于美国、加拿大和欧洲普遍以ISO 9001, EN 46001或ISO 13485作为****体系的要求,故建议****体系的建立均以这些标准为基础。
展开全文

